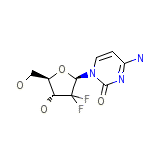
Gemcitabine hydrochloride




Categorie
Gemcitabine hydrochloride Les marques, Gemcitabine hydrochloride Analogs
Gemcitabine hydrochloride Les marques melange
Gemcitabine hydrochloride Formule chimique
C9H11F2N3O4
Gemcitabine hydrochloride RX lien
http://www.rxlist.com/cgi/generic/gemcitab.htm
Gemcitabine hydrochloride FDA fiche
Gemcitabine hydrochloride msds (fiche de securite des materiaux)
Gemcitabine hydrochloride Synthese de reference
Aucune information disponible
Gemcitabine hydrochloride Poids moleculaire
263.198 g/mol
Gemcitabine hydrochloride Point de fusion
168.64oC
Gemcitabine hydrochloride H2O Solubilite
Solubles
Gemcitabine hydrochloride Etat
Solid
Gemcitabine hydrochloride LogP
-1.318
Gemcitabine hydrochloride Formes pharmaceutiques
Poudre lyophilisée pour injection
Gemcitabine hydrochloride Indication
Pour le traitement de première ligne de patients atteints de cancer du sein métastatique, localement avancé (stade IIIA ou IIIB), ou métastatique (stade IV) non-small cell lung cancer et comme traitement de première ligne pour les patients atteints d'un adénocarcinome du pancréas.
Gemcitabine hydrochloride Pharmacologie
La gemcitabine est un antinéoplasique anti-métabolite. Anti-métabolites déguiser en purine ou pyrimidine - qui deviennent les éléments constitutifs de l'ADN. Ils empêcheront que ces substances deviennent intégrés dans d' ADN pendant le "S" de phase (ou phase de synthèse d'ADN du cycle cellulaire), l'arrêt du développement normal et la division. La gemcitabine bloque une enzyme qui convertit le nucléotide cytosine dans le dérivé désoxy. . En outre, la synthèse d'ADN est encore inhibé, car les blocs gemcitabine l'incorporation de la thymidine nucléotides dans le brin d'ADN.
Gemcitabine hydrochloride Absorption
100%
Gemcitabine hydrochloride Toxicite
La myélosuppression, des paresthésies et des éruptions cutanées sévères ont été les toxicités principales, DL50 = 500 mg / kg (par voie orale chez la souris et rats)
Gemcitabine hydrochloride Information pour les patients
General �� Patients receiving therapy with Gemzar should be monitored closely by a physician
experienced in the use of cancer chemotherapeutic agents. Most adverse events are reversible and
do not need to result in discontinuation, although doses may need to be withheld or reduced.
There was a greater tendency in women, especially older women, not to proceed to the next
cycle.
Laboratory Tests �� Patients receiving Gemzar should be monitored prior to each dose with a
complete blood count (CBC), including differential and platelet count. Suspension or
modification of therapy should be considered when marrow suppression is detected.
experienced in the use of cancer chemotherapeutic agents. Most adverse events are reversible and
do not need to result in discontinuation, although doses may need to be withheld or reduced.
There was a greater tendency in women, especially older women, not to proceed to the next
cycle.
Laboratory Tests �� Patients receiving Gemzar should be monitored prior to each dose with a
complete blood count (CBC), including differential and platelet count. Suspension or
modification of therapy should be considered when marrow suppression is detected.
Gemcitabine hydrochloride Organismes affectes
Les humains et autres mammifères