Becenun




Categorie
Becenun Les marques, Becenun Analogs
Becenun Les marques melange
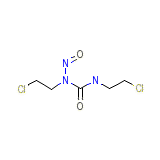
Becenun Formule chimique
C5H9Cl2N3O2
Becenun RX lien
http://www.rxlist.com/cgi/generic3/carmustine.htm
Becenun FDA fiche
Becenun msds (fiche de securite des materiaux)
Becenun Synthese de reference
Johnston TP et al. J Med Chem 122:669-681 (1963).
Becenun Poids moleculaire
214.049 g/mol
Becenun Point de fusion
31 oC
Becenun H2O Solubilite
<0.1 g/100 ml à 18 ° C
Becenun Etat
Solid
Becenun LogP
1.256
Becenun Formes pharmaceutiques
Poudre pour solution; Wafer
Becenun Indication
Pour le traitement des tumeurs cérébrales, le myélome multiple, maladie de Hodgkin et les lymphomes non-hodgkiniens.
Becenun Pharmacologie
La carmustine est l'un des nitrosourées indiqué comme traitement palliatif comme monothérapie ou en thérapie combinée établis avec d'autres agents chimiothérapeutiques homologués dans le traitement des tumeurs cérébrales, de multiples myélome, maladie de Hodgkin et les lymphomes non hodgkiniens. Bien qu'il soit généralement admis que la carmustine alkylats ADN et l'ARN, il n'est pas résistant à croiser avec d'autres alkylators. Comme avec les autres nitrosourées, , Il peut aussi inhiber plusieurs grands processus enzymatiques par carbamoylation des acides aminés dans les protéines.
Becenun Absorption
5 à 28% la biodisponibilité
Becenun Toxicite
La DL50 orale chez le rat et la souris sont de 20 mg / kg et 45 mg / kg, respectivement. Les effets secondaires incluent une leucopénie, thrombocytopénie, nausées. Les effets toxiques comprennent la fibrose pulmonaire (20-0%) et la toxicité de moelle osseuse.
Becenun Information pour les patients
No information avaliable
Becenun Organismes affectes
Les humains et autres mammifères