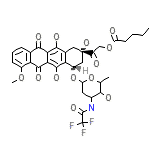
Valstar




Categorie
Valstar Les marques, Valstar Analogs
Valstar Les marques melange
Valstar Formule chimique
C34H36F3NO13
Valstar RX lien
http://www.rxlist.com/cgi/generic2/rubicin.htm
Valstar FDA fiche
Valstar msds (fiche de securite des materiaux)
Valstar Synthese de reference
Aucune information disponible
Valstar Poids moleculaire
723.644 g/mol
Valstar Point de fusion
116-117oC
Valstar H2O Solubilite
insolubles
Valstar Etat
Solid
Valstar LogP
3.332
Valstar Formes pharmaceutiques
Liquid
Valstar Indication
Cancer de la vessie
Valstar Pharmacologie
Lorsque 800 mg a été administré par voie intravésicale Valstar aux patients atteints de carcinome in situ, Valstar pénétré dans la paroi vésicale. La concentration totale moyenne mesurée anthracycline dans le tissu vésical dépassé les niveaux causant cytotoxicité de 90% à cellules de la vessie humaines cultivées in vitro. Durant les deux heures la dose la période de rétention, le métabolisme de la Valstar à ses principaux métabolites N-trifluoroacetyladriamycin et N-trifluoroacetyladriamycinol était négligeable. Après la rétention, le médicament a été presque complètement excrété par annuler la instillation. Taux de récupération moyen pour cent de Valstar, la N-trifluoroacetyladriamycin, et le total des anthracyclines dans 14 échantillons d'urine provenant de six patients était de 98,6%, 0,4% et 99,0% du total des médicaments administrés, respectivement. Durant les deux heures la dose la période de rétention, les quantités nanogramme seulement Valstar ont été absorbés dans le plasma.
Valstar Absorption
Aucune information disponible
Valstar Toxicite
Aucune information disponible
Valstar Information pour les patients
Valstar Organismes affectes
Les humains et autres mammifères