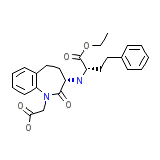
Cibacen




Categorie
Cibacen Les marques, Cibacen Analogs
Cibacen Les marques melange
Cibacen Formule chimique
Cibacen RX lien
Cibacen FDA fiche
Cibacen msds (fiche de securite des materiaux)
Cibacen Synthese de reference
Cibacen Poids moleculaire
Cibacen Point de fusion
Cibacen H2O Solubilite
Cibacen Etat
Cibacen LogP
Cibacen Formes pharmaceutiques
Cibacen Indication
Cibacen Pharmacologie
Cibacen Absorption
Cibacen Toxicite
Cibacen Information pour les patients
Pregnancy
Female patients of childbearing age should be told about the consequences of second- and third-trimester exposure to ACE inhibitors, and they should also be told that these consequences do not appear to have resulted from intrauterine ACE inhibitor exposure that has been limited to the first trimester. These patients should be asked to report pregnancies to their physicians as soon as possible.
Angioedema
Angioedema, including laryngeal edema, can occur at any time with treatment with ACE inhibitors. Patients should be so advised and told to report immediately any signs or symptoms suggesting angioedema (swelling of face, eyes, lips, or tongue, or difficulty in breathing) and to take no more drug until they have consulted with the prescribing physician.
Symptomatic Hypotension
Patients should be cautioned that lightheadedness can occur, especially during the first days of therapy, and it should be reported to the prescribing physician. Patients should be told that if syncope occurs, Lotensin should be discontinued until the prescribing physician has been consulted.
All patients should be cautioned that inadequate fluid intake or excessive perspiration, diarrhea, or vomiting can lead to an excessive fall in blood pressure, with the same consequences of lightheadedness and possible syncope.
Hyperkalemia
Patients should be told not to use potassium supplements or salt substitutes containing potassium without consulting the prescribing physician.
Neutropenia
Patients should be told to promptly report any indication of infection (e.g., sore throat, fever), which could be a sign of neutropenia.