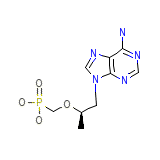
Tenofovir




Categorie
Tenofovir Les marques, Tenofovir Analogs
Tenofovir Les marques melange
Tenofovir Formule chimique
C9H14N5O4P
Tenofovir RX lien
http://www.rxlist.com/cgi/generic/viread.htm
Tenofovir FDA fiche
Tenofovir msds (fiche de securite des materiaux)
Tenofovir Synthese de reference
Aucune information disponible
Tenofovir Poids moleculaire
287.213 g/mol
Tenofovir Point de fusion
276-280oC
Tenofovir H2O Solubilite
13,4 mg / mL dans l'eau distillée à 25 ° C (fumarate de sel)
Tenofovir Etat
Solid
Tenofovir LogP
0.01
Tenofovir Formes pharmaceutiques
Comprimés pour administration orale (300 mg)
Tenofovir Indication
Pour une utilisation en combinaison avec d'autres agents antirétroviraux, pour le traitement du VIH-1.
Tenofovir Pharmacologie
Le ténofovir appartient à une classe de médicaments antirétroviraux connu comme analogue nucléotidique de la transcriptase inverse de la sérotonine (INtTI), qui bloquent la transcriptase inverse, une enzyme essentielle à la production virale dans les Personnes infectées au VIH. Le ténofovir est actuellement en phase avancée des essais cliniques pour le traitement de l'hépatite B. fumarate de ténofovir disoproxil est un analogue nucléosidique acyclique diester phosphonate de l'adénosine monophosphate. Le ténofovir nécessite une hydrolyse initiale du diester pour la conversion en ténofovir et des phosphorylations subséquentes par des enzymes cellulaires pour former le ténofovir diphosphate. Le ténofovir diphosphate est un faible inhibiteur de l'ADN polymérases α, β de mammifères, et mitochondrial ADN polymérase γ.
Tenofovir Absorption
La biodisponibilité orale chez les patients à jeun est d'environ 25%. L'administration de nourriture (repas riche en graisses contenant de 40 à 50% de graisse) augmente la biodisponibilité orale, avec une augmentation de l'AUC de 40% environ.
Tenofovir Toxicite
L'expérience clinique limitée, à des doses supérieures à la dose thérapeutique de 300 mg de ténofovir est disponible. Dans l'étude 901 ténofovir disoproxil fumarate 600 mg a été administré à 8 patients par voie orale pendant 28 jours. Aucun effet indésirable grave n'a été rapporté. Les effets de doses plus élevées ne sont pas connus.
Tenofovir Information pour les patients
Tenofovir Organismes affectes
Virus d'immunodéficience humaine