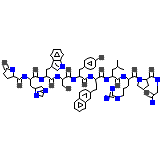
Moexipril HCL




Categorie
Moexipril HCL Les marques, Moexipril HCL Analogs
Moexipril HCL Les marques melange
Moexipril HCL Formule chimique
C66H83N17O13
Moexipril HCL RX lien
http://www.rxlist.com/cgi/generic2/nafarelin.htm
Moexipril HCL FDA fiche
Moexipril HCL msds (fiche de securite des materiaux)
Moexipril HCL Synthese de reference
Aucune information disponible
Moexipril HCL Poids moleculaire
1321.6344 g/mol
Moexipril HCL Point de fusion
No information avaliable
Moexipril HCL H2O Solubilite
Aucune information disponible
Moexipril HCL Etat
Solid
Moexipril HCL LogP
No information avaliable
Moexipril HCL Formes pharmaceutiques
Liquid;-doseur (aérosol)
Moexipril HCL Indication
Pour le traitement de la gonadotrophine-dépendant puberté précoce chez les enfants des deux sexes et pour le traitement de l'endométriose.
Moexipril HCL Pharmacologie
Nafaréline est un analogue puissant agoniste de la gonadolibérine (GnRH). Au début de l'administration, la nafaréline stimule la libération de gonadotrophines de l'hypophyse, LH et FSH, résultant en une augmentation temporaire de la stéroïdogenèse gonadique. L'administration répétée abolit l'effet stimulateur sur l'hypophyse. L'administration biquotidienne conduit à une sécrétion des stéroïdes gonadiques diminué par environ 4 semaines, par conséquent, les tissus et les fonctions qui dépendent de stéroïdes gonadiques pour leur entretien deviennent quiescentes. Après la thérapie nafaréline est interrompu, l'hypophyse et de normaliser la fonction ovarienne et l'estradiol concentrations sériques augmentent à des niveaux de prétraitement. Les récurrences de l'endométriose sont fréquentes après la cessation de tout traitement hormonal et après la chirurgie qui laisse les ovaires et / ou de l'utérus intacte.
Moexipril HCL Absorption
Rapidement absorbé dans la circulation systémique après administration intranasale. La biodisponibilité d'une dose de 400 pg de 2,8% (allant de 1,2 à 5,6%). Non absorbé après administration orale.
Moexipril HCL Toxicite
Dans les animaux de laboratoire, une administration sous-cutanée unique de 60 fois la dose recommandée chez l'homme (sur une base mg / kg, non corrigée des biodisponibilité) n'a eu aucun effet indésirable. A l'heure actuelle, il n'existe pas de preuves cliniques d'effets indésirables suite d'un surdosage d'analogues de la GnRH.
Moexipril HCL Information pour les patients
Moexipril HCL Organismes affectes
Les humains et autres mammifères