DEA No. 9720




Categorie
DEA No. 9720 Les marques, DEA No. 9720 Analogs
DEA No. 9720 Les marques melange
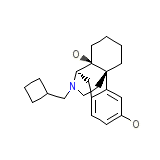
DEA No. 9720 Formule chimique
C21H29NO2
DEA No. 9720 RX lien
http://www.rxlist.com/cgi/generic2/butor.htm
DEA No. 9720 FDA fiche
DEA No. 9720 msds (fiche de securite des materiaux)
DEA No. 9720 Synthese de reference
Aucune information disponible
DEA No. 9720 Poids moleculaire
327.461 g/mol
DEA No. 9720 Point de fusion
No information avaliable
DEA No. 9720 H2O Solubilite
Modérée
DEA No. 9720 Etat
Solid
DEA No. 9720 LogP
4.176
DEA No. 9720 Formes pharmaceutiques
Gouttes; prémélange médicamenteux; Gel; Globules; Liquide; Poudre pour solution; Solution; pulvérisation; Tablet
DEA No. 9720 Indication
Pour la gestion de la douleur lors de l'utilisation d'un analgésique opioïde est approprié. Également indiqué comme médicament préopératoire ou pré-anesthésique, comme un complément à l'anesthésie équilibrée, et pour le soulagement de la douleur pendant le travail.
DEA No. 9720 Pharmacologie
Le butorphanol est un opioïde synthétique agoniste-antagoniste antalgique avec un profil pharmacologique et thérapeutique qui a été bien établi depuis son lancement comme une formulation parentérale, en 1978. L'introduction d'une formulation transnasale du butorphanol représente une nouvelle présentation et non invasive d'un analgésique pour la douleur modérée à sévère. Cette voie d'administration contourne le tractus gastro-intestinal, et cela est un avantage pour un médicament comme le butorphanol qui subit significative métabolisme de premier passage après administration orale. Le début d'action et la biodisponibilité systémique de la suite butorphanol la livraison transnasale sont similaires à ceux rapportés après administration parentérale. Butorphanol blocs impulsions de douleur sur des sites spécifiques dans le cerveau et la moelle épinière.
DEA No. 9720 Absorption
Rapidement absorbé après injection intramusculaire et des concentrations plasmatiques maximales sont atteintes en 20-40 minutes. La biodisponibilité absolue est de 60-70% et est inchangée chez les patients atteints de rhinite allergique. Chez les patients l'aide d'un vasoconstricteur nasal (oxymétazoline) la fraction de la dose absorbée est resté inchangé, mais le taux d'absorption a été ralentie. La biodisponibilité orale est seulement 5-17% en raison d'effet de premier passage métabolisme.
DEA No. 9720 Toxicite
Les manifestations cliniques de surdosage butorphanol sont ceux des opiacés en général. Les symptômes les plus graves sont l'hypoventilation, insuffisance cardio-vasculaire, un coma et la mort.
DEA No. 9720 Information pour les patients
DEA No. 9720 Organismes affectes
Les humains et autres mammifères