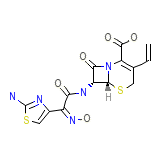
Omnicef (TN)




Categoria
Omnicef (TN) Nombres de marca, Omnicef (TN) Analogos
Omnicef (TN) Marca los nombres de mezcla
Omnicef (TN) Formula quimica
C14H13N5O5S2
Omnicef (TN) RX enlace
http://www.rxlist.com/cgi/generic2/cefdin.htm
Omnicef (TN) FDA hoja
Omnicef (TN) MSDS (hoja de seguridad de materiales)
Omnicef (TN) Sintesis de referencia
No hay información disponible
Omnicef (TN) Peso molecular
395.416 g/mol
Omnicef (TN) Punto de fusion
No information avaliable
Omnicef (TN) H2O Solubilidad
No hay información disponible
Omnicef (TN) Estado
Solid
Omnicef (TN) LogP
0.657
Omnicef (TN) Formas de dosificacion
Cápsulas de administración oral (300 mg), la suspensión oral (125 mg por 5 ml solución)
Omnicef (TN) Indicacion
Para el tratamiento de las vías respiratorias, piel, tejidos blandos, e infecciones de ENT causada por H. influenzae (incluyendo b-lactamasas cepas productoras), H. parainfluenzae (incluyendo b-lactamasas cepas productoras) ), S. pneumoniae (cepas sensibles a la penicilina), S. pyogenes, S. aureus (incluyendo b-lactamasas de las cepas que producen), y M. catarrhalis.
Omnicef (TN) Farmacologia
Cefdinir es una cefalosporina de tercera generación con un amplio espectro de actividad contra entérica gram-negativos. Cefdinir es estable en presencia de algunos, pero no todas, las enzimas b-lactamasas. Como resultado de ello, muchos organismos resistentes a las penicilinas y algunas cefalosporinas son susceptibles a cefdinir. Cefalosporinas de trabajo de la misma manera como las penicilinas: interfieren con la síntesis de peptidoglicano de las bacterias pared mediante la inhibición de la transpeptidación final, necesaria para los enlaces cruzados. Este efecto es bactericida.
Omnicef (TN) Absorcion
Concentraciones máximas en plasma se producen cefdinir 2 a 4 horas después de la dosis después de la cápsula o la administración de la suspensión. Biodisponibilidad estimada de las cápsulas de cefdinir es del 21% tras la administración de un 300 mg de dosis de cápsulas, y un 16% tras la administración de una dosis de 600 mg cápsulas. Biodisponibilidad absoluta estimada de la suspensión de cefdinir es del 25%. Absorción se reduce en aproximadamente un 15% cuando se administra con una comida rica en grasas.
Omnicef (TN) Toxicidad
Información sobre la sobredosis cefdinir en humanos no está disponible. En los estudios de toxicidad de los roedores, una sola dosis oral de 5600-mg/kg no produjo efectos adversos. Signos y síntomas tóxicos tras una sobredosis con otros antibióticos b-lactámicos, que incluyen náuseas, vómito, malestar epigástrico, diarrea y convulsiones.
Omnicef (TN) Informacion de Pacientes
Omnicef (TN) Organismos afectados
Entéricas gram-negativos