SUD919CL2Y




Categoria
SUD919CL2Y Marchi, SUD919CL2Y Analoghi
SUD919CL2Y Marchi miscela
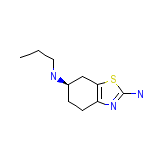
SUD919CL2Y Formula chimica
SUD919CL2Y RX link
SUD919CL2Y FDA foglio
SUD919CL2Y DMS (foglio di materiale di sicurezza)
SUD919CL2Y Sintesi di riferimento
SUD919CL2Y Peso molecolare
SUD919CL2Y Temperatura di fusione
SUD919CL2Y H2O Solubilita
SUD919CL2Y Stato
SUD919CL2Y LogP
SUD919CL2Y Forme di dosaggio
SUD919CL2Y Indicazione
SUD919CL2Y Farmacologia
SUD919CL2Y Assorbimento
SUD919CL2Y Tossicita
SUD919CL2Y Informazioni paziente
Patients should be instructed to take MIRAPEX only as prescribed.
Patients should be informed that hallucinations can occur and that the elderly are at a higher risk than younger patients with Parkinson 's disease.
Patients may develop postural (orthostatic) hypotension, with or without symptoms such as dizziness, nausea, fainting or blackouts, and sometimes, sweating. Hypotension may occur more frequently during initial therapy. Accordingly, patients should be cautioned against rising rapidly after sitting or lying down, especially if they have been doing so for prolonged periods and especially at the initiation of treatment with MIRAPEX.
Patients should be advised that MIRAPEX may cause somnolence and that they should neither drive a car nor operate other complex machinery until they have gained sufficient experience on MIRAPEX to gauge whether or not it affects their mental and/or motor performance adversely. Because of the possible additive sedative effects, caution should also be used when patients are taking other CNS depressants in combination with MIRAPEX.
Because the teratogenic, potential of pramipexole has not been completely established in laboratory animals, and because experience in humans is limited, patients should be advised to notify their physicians if they become pregnant or intend to become pregnant during therapy.
Because of the possibility that pramipexole may be excreted in breast milk, patients should be advised to notify their physicians if they intend to breast-feed or are breast-feeding an infant.
If patients develop nausea, they should be advised that taking MIRAPEX with food may reduce the occurrence of nausea.