SCM




Categoria
SCM Marchi, SCM Analoghi
SCM Marchi miscela
SCM Formula chimica
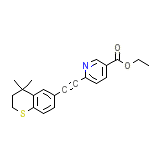
C21H21NO2S
SCM RX link
http://www.rxlist.com/cgi/generic3/avage.htm
SCM FDA foglio
SCM DMS (foglio di materiale di sicurezza)
SCM Sintesi di riferimento
Nessuna informazione disponibile
SCM Peso molecolare
351.463 g/mol
SCM Temperatura di fusione
No information avaliable
SCM H2O Solubilita
Solubile
SCM Stato
Solid
SCM LogP
5.96
SCM Forme di dosaggio
Crema o gel (0,05% o 0,1%)
SCM Indicazione
Utilizzati per il trattamento della psoriasi, acne e sole la pelle danneggiata (fotodanneggiamento).
SCM Farmacologia
Tazarotene è un profarmaco e un membro della classe dei retinoidi acetilenici. A seguito di applicazione topica, Tazarotene subisce idrolisi esterasi per formare il suo metabolita attivo, acido tazarotenic. Quando Tazarotene nel trattamento dell'acne può essere preso in concomitanza con un antibiotico orale. Tazarotene è stato dimostrato in studi peer-reviewed doppio cieco per ridurre: chiazze e iperpigmentazione, sallowness, multa rughe e rughe grossolane in pelle danneggiata dal sole. Studi istologici hanno dimostrato che a lungo termine (oltre 1 anno) l'uso del Tazarotene è associato ad una significativa riduzione nei melanociti atipici e cheratociti - le cellule considerate precursori di cancro della pelle. Alcuni studi hanno dimostrato l'uso a lungo termine del Tazarotene per essere associate a una maggiore produzione di collagene e una migliore organizzazione della pelle fasci di collagene.
SCM Assorbimento
Minimo assorbimento sistemico di Tazarotene si verifica a causa della sua rapido metabolismo della pelle al metabolita attivo, l'acido tazarotenic, che può essere assorbito e metabolizzato ulteriormente. Genere ha avuto alcuna influenza sulla biodisponibilità sistemica di acido tazarotenic.
SCM Tossicita
Eccessivo uso topico può portare ad arrossamenti marcati, peeling, o di disagio. Ingestione orale del farmaco può influenzare la funzione del fegato provocando ipertrigliceridemia. Altri sintomi possono includere irritazione congiuntivale, perdita di capelli, mal di testa, edema, stanchezza, dermatite, nausea e disturbi visivi. La somministrazione orale di questo materiale per ratti e conigli a dosi di 0,20 mg / kg / die (conigli) e 0,25 mg / kg / die (ratti) ) È risultato tossico sviluppo. Una dose senza effetto di 0,05 mg / kg / die è stato stabilito. Simili effetti teratogeni sono stati segnalati per i composti retinoidi altri.
SCM Informazioni paziente
SCM Atto interessato organismi
Gli esseri umani e altri mammiferi