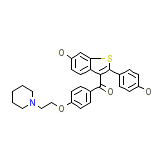
Raloxifene Hydrochloride




Categorie
Raloxifene Hydrochloride Les marques, Raloxifene Hydrochloride Analogs
Raloxifene Hydrochloride Les marques melange
Raloxifene Hydrochloride Formule chimique
C28H27NO4S
Raloxifene Hydrochloride RX lien
http://www.rxlist.com/cgi/generic/raloxif.htm
Raloxifene Hydrochloride FDA fiche
Raloxifene Hydrochloride msds (fiche de securite des materiaux)
Raloxifene Hydrochloride Synthese de reference
CD Jones et al., J. Med. Cem. 27, 1057 (1984)
Raloxifene Hydrochloride Poids moleculaire
473.584 g/mol
Raloxifene Hydrochloride Point de fusion
143-147oC
Raloxifene Hydrochloride H2O Solubilite
0.25mg / L
Raloxifene Hydrochloride Etat
Solid
Raloxifene Hydrochloride LogP
5.749
Raloxifene Hydrochloride Formes pharmaceutiques
Tablet
Raloxifene Hydrochloride Indication
Pour la prévention de l'ostéoporose chez les femmes post-ménopausées
Raloxifene Hydrochloride Pharmacologie
Le raloxifène, un modulateur sélectif des récepteurs d'œstrogènes (SERM) de la classe benzothiophène, est similaire au tamoxifène en ce qu'elle produit de l'oestrogène-like effets sur les os et le métabolisme des lipides, tandis que contrarier les effets des œstrogènes sur les tissus mammaires. Le raloxifène diminue la résorption osseuse, augmente la densité minérale osseuse (DMO) et diminue l'incidence des fractures. Le raloxifène est utilisé dans la prévention de l'ostéoporose l'ostéoporose et le cancer du sein.
Raloxifene Hydrochloride Absorption
Environ 60% d'une dose orale est absorbée, mais glycuroconjugaison présystémique est vaste. La biodisponibilité absolue du raloxifène est de 2,0%
Raloxifene Hydrochloride Toxicite
Aucune information disponible
Raloxifene Hydrochloride Information pour les patients
PATIENT INFORMATION
For safe and effective use of EVISTA, the physician should inform patients about the following:
Patient Immobilization: EVISTA should be discontinued at least 72 hours prior to and during prolonged immobilization
(e.g., post-surgical recovery, prolonged bed rest), and patients should be advised to avoid prolonged restrictions of
movement during travel because of the increased risk of venous thromboembolic events.
Hot flashes or flushes: EVISTA is not effective in reducing hot flashes or flushes associated with estrogen deficiency.
In some asymptomatic patients, hot flashes may occur upon beginning EVISTA therapy.
Other Preventive Measures: Patients should be instructed to take supplemental calcium and vitamin D, if daily dietary
intake is inadequate. Weight-bearing exercise should be considered along with the modification of certain behavioral
factors, such as cigarette smoking, and/or alcohol consumption, if these factors exist.
Physicians should instruct their patients to read the patient package insert before starting therapy with EVISTA and to
re-read it each time the prescription is renewed.
For safe and effective use of EVISTA, the physician should inform patients about the following:
Patient Immobilization: EVISTA should be discontinued at least 72 hours prior to and during prolonged immobilization
(e.g., post-surgical recovery, prolonged bed rest), and patients should be advised to avoid prolonged restrictions of
movement during travel because of the increased risk of venous thromboembolic events.
Hot flashes or flushes: EVISTA is not effective in reducing hot flashes or flushes associated with estrogen deficiency.
In some asymptomatic patients, hot flashes may occur upon beginning EVISTA therapy.
Other Preventive Measures: Patients should be instructed to take supplemental calcium and vitamin D, if daily dietary
intake is inadequate. Weight-bearing exercise should be considered along with the modification of certain behavioral
factors, such as cigarette smoking, and/or alcohol consumption, if these factors exist.
Physicians should instruct their patients to read the patient package insert before starting therapy with EVISTA and to
re-read it each time the prescription is renewed.
Raloxifene Hydrochloride Organismes affectes
Les humains et autres mammifères