DEA No. 9720




Categoria
DEA No. 9720 Nombres de marca, DEA No. 9720 Analogos
DEA No. 9720 Marca los nombres de mezcla
DEA No. 9720 Formula quimica
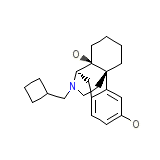
C21H29NO2
DEA No. 9720 RX enlace
http://www.rxlist.com/cgi/generic2/butor.htm
DEA No. 9720 FDA hoja
DEA No. 9720 MSDS (hoja de seguridad de materiales)
DEA No. 9720 Sintesis de referencia
No hay información disponible
DEA No. 9720 Peso molecular
327.461 g/mol
DEA No. 9720 Punto de fusion
No information avaliable
DEA No. 9720 H2O Solubilidad
Moderado
DEA No. 9720 Estado
Solid
DEA No. 9720 LogP
4.176
DEA No. 9720 Formas de dosificacion
Gotas, premezcla de Drogas; Gel, glóbulos, líquido, polvo para solución, solución, spray, Tablet
DEA No. 9720 Indicacion
Para el tratamiento del dolor cuando el uso de un analgésico opioide es apropiado. También está indicado como una medicación preoperatorio o preanestésico, como un suplemento a la anestesia equilibrada, y para el alivio del dolor durante el parto.
DEA No. 9720 Farmacologia
El butorfanol es un opioide sintético agonista-antagonista analgésico con un perfil farmacológico y terapéutico que ha sido bien establecida desde su lanzamiento como una formulación parenteral en 1978. La introducción de una formulación de butorfanol transnasal representa una nueva presentación y no invasiva de un analgésico para el dolor moderado a severo. Esta vía de administración no pasa por el tracto gastrointestinal, y esto es una ventaja para un fármaco como el butorfanol que sufre importantes metabolismo de primer paso después de la administración oral. El inicio de acción y la biodisponibilidad sistémica de la siguiente butorfanol entrega transnasal son similares a los de la administración parenteral. Bloques de butorfanol los impulsos de dolor en los sitios específicos en el cerebro y la médula espinal.
DEA No. 9720 Absorcion
Absorbe rápidamente después de la inyección intramuscular y los niveles plasmáticos máximos se alcanzan en 20-40 minutos. La biodisponibilidad absoluta es del 60-70% y no ha cambiado en los pacientes con rinitis alérgica. En los pacientes con un vasoconstrictor nasal (oximetazolina), la fracción de la dosis absorbida se mantuvo sin cambios, pero la tasa de absorción lenta fue. La biodisponibilidad oral es sólo 5.17% por extenso de primer paso metabolismo.
DEA No. 9720 Toxicidad
Las manifestaciones clínicas de la sobredosis de butorfanol son los de los opiáceos en general. Los síntomas más graves son la hipoventilación, insuficiencia cardiovascular, coma y muerte.
DEA No. 9720 Informacion de Pacientes
DEA No. 9720 Organismos afectados
Humanos y otros mamíferos